
Тел.: +7 (383) 330-67-71, факс: +7 (383) 330-80-56, E-mail: bic@catalysis.ru
630090, Россия, Новосибирск, пр-т Ак. Лаврентьева, 5

Тел.: +7 (383) 330-67-71, факс: +7 (383) 330-80-56, E-mail: bic@catalysis.ru
630090, Россия, Новосибирск, пр-т Ак. Лаврентьева, 5
МОДУЛЬНАЯ ПРОГРАММА ЛЕКЦИОННОГО КУРСА, СЕМИНАРОВ И САМОСТОЯТЕЛЬНОЙ РАБОТЫ СТУДЕНТОВ
Методическое пособие, предназначенное для студентов III курса ФЕН специальности «Химия», содержит программу курса лекций в 5-м семестре, структуру курса и правила ИКИ. Кроме того, приведен набор задач для самостоятельной работы студентов (домашних заданий) и даны примеры вариантов промежуточных и экзаменационных контрольных работ за прошлые годы.
Составитель д-р хим. наук, доц. А. А. Хасин
© Новосибирский государственный университет, 2009
Для просмотра web-документов, содержащих формулы, представленные в MathML, и подготовленных указанным выше способом, необходимо наличие на вашем компьютереЗадача 1 (80 баллов)
Рассчитайте равновесное парциальное давление аммиака, если его синтез проводят из азота и водорода при H2:N2 = 3
при постоянном давлении 160 атм и температуре 700 K. Зависимостью теплоемкости от температуры можно пренебречь. При расчете учтите, что коэффициенты
летучести аммиака, водорода и азота для равновесного состава смеси в условиях реакции составляют соответственно 0,93, 0,95 и 0,96.
|
кДж/моль |
Дж/(моль.) |
Дж/(мольК) |
|
|
H2 NH3 |
0 – 45,9 |
130,7 192,8 |
28,8 35,7 |
Задача 2 (80 баллов)
При температуре 400 K получена равновесная газовая реакционная смесь A2 и А, в которой оба вещества представлены в равных мольных
количествах. Суммарное давление полученной смеси равно 2 бар. Определите энтальпию диссоциации А2, если известно, что после изохорного
нагревания до температуры 500 K количество молей димера А2 в новой равновесной смеси уменьшилось в два раза.
Задача 3 (80 баллов)
Замечено, что в диапазоне температур от 10°С до 25°С давление насыщенных паров воды приблизительно следует правилу: “сколько градусов – столько
мм рт. ст.”. Оцените теплоту испарения воды и температуру кипения воды при атмосферном давлении.
Задача 4 (80 баллов)
Коэффициенты активности γi компонент бинарного раствора описываются уравнениями
типа ln(γi)= bi /T, где b1 = 35 К и b2 = 65 К.
Приготовлен эквимолярный раствор. Рассчитайте молярную энтропию и молярную энтальпию смешения. Определите температуру полученного раствора,
приняв исходную температуру обеих компонент (до смешения) равной 20 оС. Известно, что мольная теплоемкость c p бинарного
эквимолярного раствора постоянна и равна 5R.
Задача 5 (80 баллов)
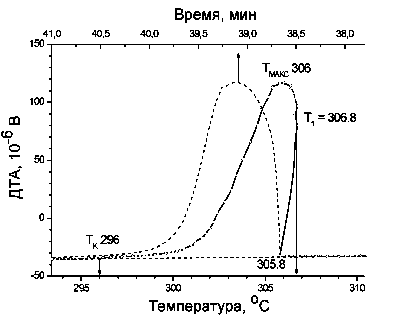
На рисунке приведен фрагмент термической кривой ДТА охлаждения NaNO3, содержащий эффект кристаллизации соли из расплава.
Пунктиром отмечена зависимость сигнала ДТА от времени (верхняя ось абсцисс). Скорость охлаждения – 5 К/мин.
Оцените размер первичных зародышей твердой фазы, если известно, что теплота плавления NaNO3 составляет 16 кДж/моль, а коэффициент поверхностного натяжения для тв. NaNO3 в контакте с расплавом можно полагать равным 0,35 Дж/м2. Плотность NaNO3 = 2,26 г/см3, молярная масса 85 г/моль.
Задача 6 (дополнительная, 100 баллов, но при условии, что в сумме не более 400 баллов)
Существование в системе уран–ртуть трех кристаллических соединений (UHg2, UHg3 и UHg4) было установлено
Рэндлом и Вилсоном (Acta Crystallogr. 1949. Vol. 3. P. 148–150). Используя данные таблицы, постройте Т–х диаграмму в диапазоне температур 250–400 К).
Известно, что Тпл урана 1403 К, Тпл ртути 234 К, твердые растворы в системе не образуются. Также известны термодинамические
характеристики реакций образования соединений U–Hg из α–урана и жидкой ртути
|
|
|
|
|
UHg3 UHg4 |
– 63,55 – 78,01 |
– 46,73 – 66,40 |